重症新冠肺炎患者的人体免疫防御路径发生“变道”,在这个过程中究竟发生了什么?3月8日,上海交通大学医学院附属仁济医院风湿科中澳个体化免疫研究中心卡罗拉·维努埃萨(Carola Vinuesa)课题组在《免疫》期刊发表评述文章,从多角度探讨人体B细胞发育路径在各种病理条件下的不同作用,为感染和自身免疫病的防治提供了新的靶点和方向。
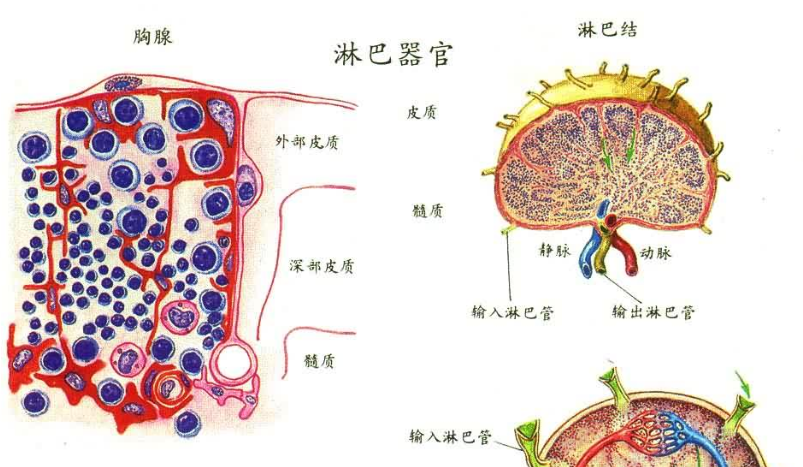
免疫系统是机体天然的防御武器,它构筑了多重防线抵御病原微生物入侵,其中B细胞介导的抗体应答是免疫系统的重要防御机制。B细胞主要通过两种路径发育成为抗体生成细胞:生发中心(GC)路径和滤泡外(EF)路径。生发中心路径通过长时程的亲和力筛选,为机体长期提供高亲和力抗体防御;滤泡外路径通常产生低亲和力抗体,为机体提供快速保护。
鼠伤寒沙门氏菌(STm)是人和动物肠道主要病原菌之一,它随污染的水和食物进入宿主,具有广泛的致病性。此病原菌非常狡猾,它会破坏B细胞生发中心应答,并影响机体产生长寿命的免疫记忆和抗体防御。
近期,以色列魏茨曼科学研究所的Adi Biram等研究人员发现,鼠伤寒沙门氏菌等细菌感染能从骨髓中募集单核细胞,并通过IFN-γ和TNF-α依赖的方式损坏B细胞代谢适应,最终抑制生发中心应答。
研究人员表示,B细胞主要通过滤泡外而非生发中心路径分化成熟,不仅常见于鼠伤寒沙门氏菌等细菌感染,还是自身免疫病如系统性红斑狼疮(SLE)致病性B细胞应答的主要特征。这种特有的联系为感染驱动自身免疫提供了重要依据。
此外,B细胞生发中心应答路径向滤泡外路径的转换是重症新型冠状病毒肺炎(COVID-19)患者的重要表型特征,是患者较差愈后的指示标。因此,深入研究B细胞发育调控的不同路径,将对感染和自身免疫病的防治产生重要影响。
专家表示,该研究论文从多角度探讨了B细胞两种发育路径在细菌、病毒感染及自身免疫病等病理条件下的不同作用,深化了人们对B细胞生发中心应答和滤泡外应答的平衡调控因素的理解,为感染和自身免疫病的防治提供了新的靶点和方向。
 营业执照公示信息
营业执照公示信息